War die $3 Mrd. Busse gegen GlaxoSmithKline ein Einzelfall? Was waren die Bussen der letzten Jahre? Welche Ermittlungen sind im Gange?
Ich bin nicht gegen Pharma, aber ich bin gegen unsaubere Machenschaften und illegale Praktiken. Die Pharmaindustrie vertreibt lebensrettende Medikamente und ist eine wichtige Industrie. Leider aber scheint der Gewinn mit allen Mitteln maximiert zu werden – mit legalen und illegalen.
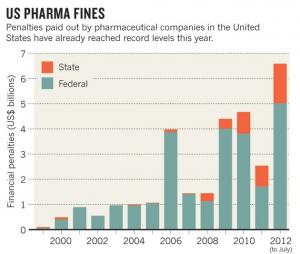
 US Bussen für Big Pharma bis Juli 2012 | CC BY-NC-ND Public Citizen
US Bussen für Big Pharma bis Juli 2012 | CC BY-NC-ND Public Citizen
Bei der Pharmaindustrie hat man manchmal den Eindruck es gehe nur ums Verkaufen – soviel und so teuer wie möglich. Ungeeignete, mittelmässige oder gar nutzlose Medikamente werden nach allen Regeln der Kunst, teilweise illegalen, an den Mann und die Frau gebracht. Es werden Ärzte, Forscher, Studien und Politiker manipuliert. Studien beschönigt, Wissenschaftlichkeit vorgetäuscht, „negative Resultate“ unterdrückt, Wirkungen übertrieben. Produktionsprozesse nicht im Griff. Überrissene Preise werden verrechnet. Bestechungsgelder (Kickbacks) an Ärzte für Verordnungen bezahlt(, welche auch angenommen wurden). Kritiker bedroht und eingeschüchtert. Nein, es handelt sich hier nicht um die Mafia.
Ich habe einmal eine Zusammenstellung der Bussen der US Justiz erstellt, zusammen mit anderen dokumentiertem Fehlverhalten. Die Liste erhebt keinen Anspruch auf Vollständigkeit.
| Unternehmen |
Grund |
Busse Mio $ |
Jahr |
Referenz |
| Novartis |
Marketingfehlverhalten, Kickbacks (Trileptal) |
422.5 |
2010 |
Tagi blog.nytimes USDOJ |
| Novartis |
Frauendiskriminierung |
250 |
2010 |
NZZ |
| Roche |
Marketingfehlverhalten und Preismanipulation (Rituxan) |
20 |
2011 |
Pharmalot |
| Pfizer |
Marketingfehlverhalten, Schmiergeld (Bextra, Lipitor, Viagra) |
2300 |
2010 |
NZZ |
| Eli Lilly |
Marketingfehlverhalten (Zyprexa) |
1400 |
2010 |
NZZ USDOJ |
| Branche |
Verzögerung, Blockierung von Generika (Bericht EU) |
|
2008 |
NZZ |
| GlaxoSmithKline |
Marketingfehlverhalten (Paxil, Wellbutrin, Avandia, Advair, Lamictal, Zofran), Kick-Backs (Imitrex, Lotronex, Flovent, Valtrex), Überzogene Rechnungen |
3000 |
2012 |
Blogartikel Tagi Spiegel USDOJ, USDOJ Pharmalot Pharmalot |
| GlaxoSmithKline |
Marketingfehlverhalten (Wellbutrin SR) |
FDA Klage |
Offen |
Pharmalot |
| Merck Serono |
Kickbacks (Rebif®) |
44.3 |
2011 |
Bloomberg, USDOJ |
| Merck KGaA |
Produktionsprobleme |
FDA Brief |
2012 |
Pharmalot |
| Merck Serono |
Marketingfehlverhalten (Serostim) |
704 |
2005 |
USDOJ |
| Bayer Healthcare |
Marketingfehlverhalten (Xarelto) |
Klage |
2012 |
Spiegel |
| Pfizer |
Marketingfehlverhalten (Neurotonin) |
141 |
2010 |
Reuters Pharmalot |
| Pfizer |
Brustkrebs (Prempro) |
45 |
2012 |
Bloomberg |
| Pfizer |
Brustkrebs (Prempro) |
10.4 |
2012 |
Bloomberg |
| Pfizer |
Brustkrebs (Prempro) |
896 |
2012 |
Bloomberg Businessweek Bloomberg |
| Pfizer |
Brustkrebs (Prempro) |
72 |
2011 |
Pharmalot |
| Pfizer |
Mutmasslich illegaler Freilandversuch an Kindern in Afrika (Trovan), Druck auf Staatsanwaltschaft |
75 |
2010 |
Süddeutsche US Cable Guardian |
| Merck (MSD) |
Marketingfehlverhalten (Vioxx®) |
C$ 37 |
2012 |
Yahoo |
| Merck (MSD) |
Marketingfehlverhalten (Vioxx®) |
950 |
2011 |
Spiegel USDOJ |
| Pfizer |
Nichtpublikation negativer Resultate (Reboxetine) |
Publ. |
2010 |
IQWiG BMJ |
| Pfizer (Wyeth) |
Ghostwriting (HRT) |
Publ. |
2010 |
Ärzteblatt |
| GlaxoSmithKline |
Produktqualität (Avandia, Paxil) und Produktionsmethoden |
750 |
2010 |
independent.co.uk |
| Elan |
Marketingfehlverhalten (Zonegran) |
203 |
2011 |
USDOJ USDOJ |
| Dey |
Preisbetrug |
280 |
2010 |
USDOJ |
| Forest |
Marketingfehlverhalten (Levothroid, Celexa, Lexapro) |
313 |
2010 |
USDOJ |
| Abott |
Marketingfehlverhalten (Depakote) |
1600 |
2012 |
USDOJ Pharmalot |
| Novo Nordisk |
Marketingfehlverhalten (Novoseven) |
25 |
2011 |
USDOJ |
| Johnson & Johnson |
Marketingfehlverhalten (Topamax) |
81 |
2010 |
USDOJ |
| Johnson & Johnson |
Marketingfehlverhalten (Risperdal) |
181 |
2012 |
Pharmalot |
| Johnson & Johnson Manager |
Nichtgenehmigte Studien mit Todesfolge |
Gefängnis 2×9M + 4M |
2011 |
Pharmalot |
| Sanofi-Aventis |
Preisbetrug |
190 |
2007 |
USDOJ |
| Novo Nordisk |
Kauf von Patientendaten (Novolin, Novolog) |
1.7 |
2011 |
USDOJ |
| AstraZeneca |
Off-Label Marketing, Kickbacks (Seroquel®) |
520 |
2010 |
NYimes NYTimes USDOJ |
| AstraZeneca |
Marketingfehlverhalten (Seroquel®) |
26 |
2012 |
Pharmalot |
| AstraZeneca |
Marketingfehlverhalten, Irreführung bei Nebenwirkungen, Nichtveröffentlichung negativer Resultate (Seroquel®) |
68.5 |
2011 |
Pharmalot |
| Bristol-Myers Squibb |
Marketingfehlverhalten |
515 |
2007 |
NYTimes Pharmalot |
| Bristol-Myers Squibb |
Bilanzmanipulation (Channel stuffing) |
300 |
2005 |
Bloomberg |
| Bristol-Myers Squibb |
Bilanzmanipulation (Channel stuffing) (Erbitux, Vanlev) |
300 |
2004 |
Bloomberg |
| Bristol-Myers Squibb Manager |
Bilanzmanipulation |
0.17 |
2012 |
Pharmalot |
| Bristol-Myers Squibb Manager |
Bilanzmanipulation |
0.4 |
2010 |
Pharmalot |
| Fresenius Kabi |
Bedrohung (HES) |
|
2012 |
Spiegel |
| GlaxoSmithKline |
Bedrohung (Avandia) |
|
1999 |
US Senate |
| Pfizer, Ranbaxy |
Generikaverzögerung, Kartellabsprache („Pay for Delay“) (Lipitor) |
Klage |
2012 |
BloombergBusinessNews |
| Deutsche Homöopathie-Union (DHU), Biologische Heilmittel Heel, Staufen Pharma, WALA Heilmittel, Weleda, Hevert |
Journalisten Diskreditierung |
|
2012 |
Süddeutsche |
| Teva Pharma |
Übertreibung der Wirkung und Sicherheit (Copaxone®) |
FDA Warning |
2012 |
FDA Letter Pharmalot |
| Teva Pharma |
Anwendungsrisiken (Propofol) |
250 |
2012 |
Bloomberg Pharmalot |
| Teva Pharma |
Anwendungsrisiken (Propofol) |
500 |
2010 |
Pharmalot |
| Ungenannt |
Erpressungsversuche der Inserenten bei Ärztezeitung |
Artikel |
2011 |
SÄZ |
| GlaxoSmithKline |
Unterdrückungsversuch kritischer Meinung (Avandia) |
Editorial |
2010 |
Euro. Heart Journal |
| Pfizer |
Korruption |
60 |
2012 |
Pharmalot SEC Pharmalot |
| Teva |
Korruption |
Untersuch (Subpoena) |
2012 |
Pharmalot |
| Bristol-Myers Squibb |
Korruption |
Untersuch (Subpoena) |
2012 |
Pharmalot |
| Johnson & Johnson |
Korruption |
70 |
2011 |
Pharmalot |
| Bayer |
Verletzung von Branchenrichtlinien (ABPI Code bei Xarelto) |
|
2012 |
InPharm |
| Bayer |
Sammelklage (Yasmin) |
402.6 |
2012 |
Bloomberg |
| Bayer |
Sammelklage (Yaz) |
610.5 |
Offen |
Bloomberg |
| Johnson & Johnson |
Marketingfehlverhalten (Risperdal) |
158 |
2012 |
Pharmalot |
| Johnson & Johnson |
Marketingfehlverhalten (Risperdal) |
327 |
2012 |
Bloomberg |
| Johnson & Johnson |
Marketingfehlverhalten (Risperdal) |
258 |
2010 |
Bloomberg Pharmalot |
| Johnson & Johnson |
Marketingfehlverhalten (Risperdal) |
1100 |
2012 |
SF.tv Handelszeitung Pharmalot |
| Bayer |
Marketingfehlverhalten (Aspirin) |
15 |
2012 |
Businessweek |
| Pfizer |
Marketingfehlverhalten (Zithromax) |
FDA Warnung |
2012 |
Pharmalot |
| Sanofi-Aventis |
Überzogene Rechnungen in Algerien (Overbilling) |
25 |
2012 |
La Tribune Pharmalot |
| Sanofi-Aventis |
Überzogene Rechnungen in Kanada (Quadrace, Pentacel) |
2.5 |
2012 |
Pharmalot |
| Roche |
Verheimlichung von Nebenwirkungen |
EMA Untersuch |
Offen |
DRS1 Pharmalot EMA |
| Fresenius Medical Care |
Selektive Information (GranuFlo) |
FDA Untersuch |
Offen |
NY Times Pharmalot |
| Johnson & Johnson |
Fehlerhafte Hüftimplantate |
0.6 |
2012 |
Businessweek |
| AstraZeneca |
Irreführung bei Nebenwirkungen (Seroquel®) |
46 |
2012 |
PharmaGossip |
| Eli Lilly |
Zahlung ohne Schuldeingeständnis, Vorwurf Marketingfehlverhalten (Zyprexa) |
45 |
|
PharmaGossip |
| Bristol-Myers Squibb |
Manager lügt vor Gericht |
Memoiren schreiben |
2012 |
WSJ Pharmalot |
| Abott |
Produktregelverstösse |
100 |
1999 |
Pharmalot |
| TAP Pharmaceutical (joint venture Abbott and Takeda Pharmaceutical) |
Manipulation Medicaid und Medicare |
875 |
2001 |
Pharmalot |
| Cetero |
CRO: Datenmanipulation und Studienfälschung, Teva betroffen |
Konkurs |
|
Pharmalot Pharmalot |
| Cypress Pharmaceutical |
Marketingfehlverhalten (Hylira, Zaclir, Zacare) |
2.8 |
2012 |
Pharmalot |
| GlaxoSmithKline |
Marketingfehlverhalten (Avandia) |
90 |
2012 |
Staatsanwalt Maryland |
| Novartis |
Anklage wegen Bestechung von Ärzten im Falle von Bluthochdruck (Lotrel, Valturna) und Diabetes (Starlix) |
Anklage |
2013 |
NZZ Tagesanzeiger Blick dailypress |
| Novartis |
Untersuch (Gilenya®, Glivec®) |
Untersuch |
2013 |
SonntagOnline |
| Pfizer |
Marketingfehlverhalten (Rapamune) |
491 |
2013 |
Forum Gesundheitspolitik DOJ |
| Johnson & Johnson |
Schmiergelder (=Korruption) und Marketingfehlverhalten (Risperdal) |
2200 |
2013 |
Tagi Bloomberg NYTimes |
| Lundbeck |
Generikaverzögerung (Kartellabsprachen, Pay for Delay) (Citalopram) |
129 |
2013 |
NZZ FAZ |
| Johnson & Johnson |
Generikaverzögerung (Kartellabsprachen, Pay for Delay) in NL (Fentanyl) |
15 |
2013 |
NZZ |
| Novartis |
Generikaverzögerung (Kartellabsprachen, Pay for Delay) in NL (Fentanyl) |
7 |
2013 |
NZZ |
| Novartis |
Korruption (Schmiergeldzahlungen) (Exjade, Myfortic) |
390 |
2015 |
Tagi SRF Tagi NZZ NZZ NZZ NZZ Tagesanzeiger justice.gov |
| Novartis |
Irreführende Werbung in Japan (Diovan) |
Klage |
2014 |
SRF Tagi NZZ |
| Novartis, Roche |
Preisabsprachen in Italien (Lucentis, Avastin) |
Ermitt. |
2014 |
Tagi |
| Novartis |
Verschwiegene Nebenwirkungen in Japan (Krebsmittel Tasigna) |
Rücktritte, Anklage |
2014 |
NZZ NZZ |
| Takeda |
Krebsrisiko verschwiegen (Actos, gegen Diabetes-2) |
6000 |
2014 |
NZZ |
| Eli Lilly |
Krebsrisiko verschwiegen (Actos, gegen Diabetes-2) |
3000 |
2014 |
NZZ |
| Servier, Teva, Lupin, Matrix Laboratories (Mylan), Niche/Unichem, Krka |
Verstoss gegen das Kartellverbot (Pay for delay) (Bluthochdruck-Medikament Perindopril) |
427,7 Mio. € |
2014 |
NZZ |
| GlaxoSmithKline |
Bestechungsvorwürfe in China |
Untersuch / Anklage |
2014 |
NZZ NZZ |
| Novartis, Roche |
Korruptionsvorwürfe in Rumänien |
Razzia |
2015 |
BZ |
| Novartis |
Korruptionsvorwürfe in der Türkei |
Untersuch |
2016 |
NZZ |
| Novartis |
Bestechungsvorwürfe |
Untersuch |
2016 |
Tagi |
| Novartis |
Schmiergeldazahlungsvorwürfe in Griechenland |
Untersuch |
2016 |
NZZ |
| Purdue Pharma |
Herunterspielen von OxyContin (Opioid) |
634.5 |
2007 |
NY Tagi |
| Novartis |
Vorwurf der Manipulation der Testdaten vor der Zulassung der Gen-Therapie Zolgensma (2 Mio. $ pro Einmaldosis) |
|
2019 |
NZZ NZZ |
| Purdue Pharma |
Vergleichszahlung wegen dem Opioid OxyContin |
270 |
2019 |
NZZ Tagi NZZ |
| Teva |
Vergelichszahlung wegen Opioid |
85 |
2019 |
NZZ Tagi |
| Johnson & Johnson |
Wiedergutmachung von Schäden durch synthetische Opioide im Gliedstaat Oklahoma, irreführender Werbung |
572 |
2019 |
NZZ Tagi |
| Merz Pharma Schweiz AG |
Illegale Vorteilsgewährung und Umsatzsteigerung (Axura) |
CEO 4000 Fr.; 10‘000 Fr. / Mitarbeiter |
2017 |
Sonntagszeitung |
| Insys |
Bestechung von Ärzten im Stil einer Gangsterbande zum Überverschreiben des Subsys-Sprays (Fentanyl, Opoidkrise) |
Gefängnis für Chefs |
2020 |
NZZ |
| Sandoz (Novartis) |
Illegale Preisabsprachen und andere kartellrechtliche Verstösse |
195 |
2020 |
NZZ |
| Novartis |
Bestechung von Ärzten von 2002 bis 2014 in den USA |
678 |
2020 |
NZZ Tagi Neu! |
Auflistung von Fehlverhalten und Bussen der Arzneimittelindustrie (Big Pharma und Homöopathie) der letzten Jahr. USDOJ = US Departement of Justice. Stand: 31.08.2012
Von 1987 bis 2011 zahlte die Pharmaindustrie für $30 Mrd. Bussen (DOJ, DOJ, Pharmalot, Pharmalot), davon in den Jahren 2009 und 2010 je $3 Mrd. Im Jahre 2012 zahlt allein GlaxoSmithKline eine Busse von $3 Mrd.
Die Bussen sind meistens als Vergleiche zwischen der US Justiz und den entsprechenden Pharmaunternehmen zustande gekommen. Die Bussen wurden also ausgehandelt. Dies ist in der US Justiz möglich. Leider sind in den wenigsten Vergleichen, interne Dokumente veröffentlicht worden, die weitergehende Einblicke in das Geschäftsgebaren gezeigt hätten.
Die vollständige Liste der Übereinkommen der US Justiz mit Unternehmen: Corporate Integrity Agreements
Weitere Fälle sind in Bearbeitung der US-Justiz, z.B. womögliche weitere $2.2 Mrd. Busse für Johnson & Johnsohn (Bloomberg). Stay tuned – wie die Amerikaner zu sagen pflegen. [Aktualisierung 05.11.2013: Johnson & Johnson zahlt nun die vermuteten $2.2 Mrd. Busse, siehe Nachtrag.]
Die grössten Pharmakonzerne der Welt
| # |
Unternehmen |
Sitz |
Umsatz (in Mrd. USD) |
| 1 |
Pfizer |
USA, New York |
57.7 |
| 2 |
Novartis |
Schweiz, Basel |
54.0 |
| 3 |
Merck & Co., Inc. (MSD) |
USA, New Jersey |
41.3 |
| 4 |
Sanofi-Aventis |
Frankreich, Paris |
37.0 |
| 5 |
Hoffmann-La Roche |
Schweiz, Basel |
34.9 |
| 6 |
GlaxoSmithKline |
Großbritannien, London |
34.4 |
| 7 |
AstraZeneca |
Großbritannien, London |
33.6 |
| 8 |
Johnson & Johnson |
USA, New Jersey |
24.4 |
| 9 |
Abbott |
USA, Illinois |
22.4 |
| 10 |
Eli Lilly and Company |
USA, Indianapolis |
21.9 |
Quelle: Wikipedia, Stand: 2012, CC BY-SA
Off-Label Marketing
Eines der häufigsten Marketingfehlverhalten ist das Off-Label Marketing. Medikamente müssen wissenschaftliche geprüft werden und werden danach von den Gesundheitsbehörden zugelassen. Die Zulassung gilt dann für die untersuchte Krankheit. Ärzte sind frei in der Anwendung der Medikamente. Sie dürfen das Medikament also auch für ungeprüfte Krankheiten einsetzen (was auch gut ist). Die Pharmaunternehmen dürfen solche nicht geprüfte Anwendungen in den US jedoch nicht vermarkten, das wird als Off-Label Marketing bezeichnet. Beispielsweise wenn die Wirksamkeit für ein Medikament nur in einer bestimmten Krankheitskonstellation nachgewiesen wurde, das Medikament aber später als allgemein wirksames Medikament anpreisen und verkauft wird.
Untergraben der Wissenschaft
Die Hersteller von pharmazeutischen Produkten haben kommerzielle Interessen. Die Wissenschaft ist dabei ein notwendiges Übel, die Wahrheitssuche nicht das eigentliche Ziel. Es sind Fälle dokumentiert, wo dem „wissenschaftlichen“ Nachweis „nachgeholfen“ wurde. Es wurden „negative Ergebnisse“ nicht publiziert. Von fünf Studien wurden nur 2 publiziert, 3/4 der untersuchten Patienten wurden unterschlagen. Das Medikament erschien so als wirksam, was aber mit allen Daten nicht nachgewiesen werden kann. (IQWiG BMJ)
Die Wissenschaft wurde noch auf vielfältige andere Arten verzerrt und verfälscht. Dokumentierte Fälle werde ich in einem separaten Artikel behandeln.
Lobbying
Die Pharmaindustrie nimmt mit druckvollem Lobbying Einfluss auf die Gesetzgebung. In den USA gibt es in Washington zweimal so viel Lobbyisten wie Parlamentarier (USA Today). Die Pharma-Lobbyorganisation PhRMA verfügt über gut gefüllte Kassen.
Auch in der Schweiz sieht die Sache nicht besser aus: Interpharma hat direkten Zugang zum Schweizer Parlament.
Lobbying wird bei den Pharmaunternehmen wahrscheinlich unter Marketing abgebucht. Novartis hat allein im letzten Jahr 15 Mrd. USD für Marketing ausgeben (Marketing Novartis).
Hilfreiche und wirksame Gesetze werden so verhindert oder verwässert.
Verzögern von Generika („Pay for delay“)
Ein weiterer Trick der Pharmaindustrie zum Abkassieren bei den öffentlichen Gesundheitssystemen ist es den Start von Generika nach Patentabläufen zu verzögern. Wie geht es? Patente sind zeitlich begrenzte Monopole. Nach dem Patentablauf kann der Markt spielen. Generika werden daher zu viel billigeren Preisen verkauft. Die Patentinhaber haben nun Absprachen mit den Generikaherstellern gemacht, damit diese noch zuwarten mit dem Verkauf ihrer Medikamente und können dabei die Monopolgewinne untereinander aufteilen (NZZ). Eine Win-Win-Situtation für die Pharmaindustrie auf Kosten der Prämien- und Steuerzähler. Das sind Absprachen gegen den freien Markt, also ein Kartell. Das ist ein Sakrileg in einer kapitalistischen Marktordnung.
Korruption
Neben den subtileren Methoden gibt es noch die ganz plumpe Korruption, z.B. mit Kickback-Zahlungen an Ärzte. Die Ärzte bekommen im Nachhinein eine „Provision“ für die Verschreibung. Je mehr Medikamente ein Arzt also verschreibt, desto mehr verdient er. Alte Patienten und chronisch kranke Patienten sind dafür besonders geeignet.
Kommentar
Die Pharmabranche präsentiert sich als grosse Wohltäterin der Menschheit. Bei genauerem Hinsehen ist vieles nicht so sauber wie es aussieht und die grossen Gewinne sind teilweise illegalem Verhalten zu verdanken. Die Bussen, obwohl sie hoch erscheinen, sind leider in keinem Verhältnis zu den Gewinnen der Pharmaunternehmen. Die Bussen werden wahrscheinlich einfach in die „Betriebskosten“ miteinkalkuliert.
Die Manager der Pharmaindustrie gehören zu den bestbezahlten der Welt überhaupt. Hohe Löhne scheinen in umgekehrtem Verhältnis zu ethischem Verhalten zu stehen.
Die obigen Beispiele zeigen das grosse manipulative Verhalten der Pharmaindustrie. Die fast unerschöpflichen finanziellen Mittel der Pharmaindustrie können eine korrumpierende Wirkung entfalten. Finanzielle Beiträge sind immer und überall willkommen.
Patientenorganisationen müssen sehr vorsichtig im Umgang mit der Pharmaindustrie sein. Die Unabhängigkeit muss gewahrt werden. Gefällikeiten durch die Industrie sind gefährlich. Die Glaubwürdigkeit kann sonst schlecht aufrecht erhalten werden. Das gleiche gilt auch für Ärzte und Wissenschaftler.
Das Sponsoring muss überdacht werden. Was nützt es einem Läufer, wenn er schneller laufen kann, dafür aber in eine verkehrte Richtung? Ein Rennen wird er sicher nicht mehr gewinnen.
Bei Inseraten oder Sponsorings sollten die Mitglieder und Betroffenen auf das unrechtmässige Verhalten des Sponsors hingewiesen werden, z.B. auf die Fehlverhalten innerhalb der letzten fünf Jahre. Auch die Inseratetarife für solche Sponsoren sollten angepasst werden, z.B. 10× den ordentlichen Tarif.
Nachträge
[Aktualisierung 23.11.2012: Die US Bürgerorganisation Public Citizen hat eine umfassende Analyse der Justizfälle erstellt: Pharmaceutical Criminal and Civil Penalties: An Update, Public Citizen, 27. Sep. 2012. Sie haben detaillierte Auswertungen gemacht. Dieser Bericht ist eine sehr gute Quelle.]
[Aktualisierung 06.03.2013: Ich habe einen Artikel über die teils massiven Qualitätsprobleme bei Medikamenten und Implantaten der Pharmaindustrie, insbesondere Johnson & Johnson, geschrieben.]
[Aktualisierung 27.04.2013: Anklage gegen Novartis in zwei Fällen wegen Bestechung von 1) Apothekern NZZ Tagesanzeiger, 2) Ärzten Tagesanzeiger]
[Aktualisierung 09.08.2013: 491 Mio $ Busse gegen Pfizer wegen Marketingfehlverhalten (Rapamune) hinzugefügt. Ref: Forum Gesundheitspolitik, DOJ]
[Aktualisierung 05.11.2013: Johnson & Johnson (Janssen) zahlt wie vermutet (Bloomberg Pharmalot) wegen Schmiergeldern (=Korruption) und Marketingfehlverhalten (Risperdal) die Busse von $2.2 Mrd. (Tagi Bloomberg NYTimes). Aber was sind schon $2.2 Mrd, wenn allein mit dem Medikament Risperdal $24 Mrd Gewinn gemacht wurden? Die illegalen Aktivitäten waren unter dem Strich wohl höchst rentabel. Wird durch diese Busse jemand zum Umdenken bewegt?]
[Aktualisierung 10.12.2013: Die EU verhängte Bussen für Generikaverzögerung (Kartellabsprachen, „Pay for delay“) über Novartis und Johnson & Johnson (Janssen) von $ 7 Mio und $ 15 Mio. beim Schmerzmittel Fentanyl. NZZ. Bussen in der EU scheinen in viel kleineren Grössenordnungen zu liegen. Seit 2008 läuft eine EU-Untersuchung. NZZ]
[Aktualisierung 10.12.2013: Im Sommer verhängte die EU bereits eine Busse von $ 129 Mio über Lundbeck wegen Generikaverzögerung (Kartellabsprachen, „Pay for delay“) beim Antidepressivum Citalopram. NZZ FAZ. Bussen in der EU scheinen in viel kleineren Grössenordnungen zu liegen. Seit 2008 läuft eine EU-Untersuchung. NZZ]
[Aktualisierung 09.01.2014: US Justiz (New York) reicht neue Klage gegen Novartis wegen Korruption bei Exjade ein SRF Tagi NZZ]
[Aktualisierung 09.01.2014: Japan reicht neue Klage gegen Novartis wegen irreführender Werbung bei Diovan ein SRF Tagi NZZ]
[Aktualisierung 14.03.2014: Lucentis: Italien leitet Ermittlungen gegen Roche- und Novartis-Manager ein, Tagesanzeiger.ch: (mrs/sda), 14. März 2014]
[Aktualisierung 06.04.2014: Verschwiegene Nebenwirkungen in Japan beim Krebsmittel Tasigna. Austausch der Chefs in Japan. NZZ]
[Aktualisierung 08.04.2014: Takeda und Eli Lilly sollen Krebsrisiko des Diabetes-2 Medikaments Actos verschwiegen haben. Total 9 Mrd Dollar Busse. NZZ, 08.04.2014]
[Aktualisierung 22.05.2014: Ermittlungen geben GlaxoSmithKline wegen Korruption in China abgeschlossen. NZZ]
[Aktualisierung 22.05.2014: Hausdurchsuchung der Niederlassung von Roche in China. NZZ]
[Aktualisierung 24.05.2014: Der häufig als Quelle benutzte Blog Pharmalot von Ed Silverman wurde 31.12.2013 leider geschlossen. Alle Pharmalot-Links funktionieren daher leider nicht mehr.]
[Aktualisierung 03.07.2014: Novartis wurde nun in Japan wegen Unregelmässigkeiten bei Studienresultaten angeklagt (Diovan) NZZ.]
[Aktualisierung 09.07.2014: Servier, Teva, Lupin, Matrix Laboratories (Mylan), Niche/Unichem und Krka werden wegen Verstosses gegen das Kartellverbot (Pay for delay) beim Bluthochdruck-Medikament Perindopril mit 427,7 Mio. € von der EU-Kommission gebüsst. NZZ]
[Aktualisierung 12.07.2014: GlaxoSmithKline: Untersuchung/Anklage wegen Bestechungsvorwürfe in China NZZ NZZ]
[Aktualisierung 21.09.2014: Dieser Blogartikel wurde in überarbeiteter Version im Magazin Albatros (PDF Seite 16, Papier Seite 12) der AG STG (Aktionsgemeinschaft Schweizer Tierversuchsgegner) abgedruckt.]
[Aktualisierung 06.08.2015: Razzien bei Roche und Novartis in Rumänien. Übernachtungen in Las Vegas getarnt als Dienstreise: Schweizer Pharmakonzernen wird in Rumänien Korruption vorgeworfen. Berner Zeitung, 05.08.2015]
[Aktualisierung 08.08.2015: Zum Wohl des Patienten oder des Konzerns?, NZZ, 08.08.2015. Prozess um Korruptionsvorwürfe um die Medikamente Exjade und Myfortic.]
[Aktualisierung 30.03.2016: Novartis, Korruptionsvorwürfe in der Türkei, Untersuchung, NZZ; Novartis, Bestechungsvorwürfe, Untersuchung, Tagi]
[Aktualisierung 06.01.2017: Novartis, Schmiergeldzahlungsvorwürfe in Griechenland, NZZ]
Aktualisierung 27.08.2019: Johnson & Johnson, Wiedergutmachung von Schäden durch synthetische Opioide im Gliedstaat Oklahoma, irreführender Werbung, 572 Mio $, NZZ]
[Aktualisierung 27.08.2019: Merz Pharma Schweiz AG, Illegale Vorteilsgewährung und Umsatzsteigerung (Axura), CEO 4000 Fr.; 10‘000 Fr. / Mitarbeiter Busse, 2017 Sonntagszeitung]
[Aktualisierung 01.08.2020: Novartis, Bestechung von Ärzten von 2002 bis 2014 in den USA, Vergleich von 678 Mio. $ NZZ Tagi]

 Hextril® Packung, der Pfeil zeigt den Schreibfehler. Photo: Patientensicht
Hextril® Packung, der Pfeil zeigt den Schreibfehler. Photo: Patientensicht